Современные возможности медикаментозного лечения ожирения - Журнал Доктор Ру
Современные возможности медикаментозного лечения ожирения
Цель статьи: освещение современных способов медикаментозного лечения ожирения.
Основные положения. Ожирение является социально значимой проблемой здравоохранения, поскольку оно ассоциировано с основными заболеваниями, лимитирующими продолжительность жизни населения. Проблема ожирения стояла перед обществом еще в период Гиппократа, однако реально эффективные средства для лечения появились только в ХХI веке. В статье представлен обзор современных медикаментозных средств снижения массы тела, разрешенных для применения в РФ. Рассмотрены вопросы их эффективности и побочных эффектов, представлен клинический случай лечения ожирения с помощью препарата лираглутид 3 мг.
Заключение. Пациенты с ожирением и избыточной массой тела должны обязательно обследоваться у врача с целью верификации ассоциированных заболеваний и назначения лечения, включая медикаментозную терапию, направленную на снижение массы тела.
Вклад авторов: Анциферов М.Б. — разработка концепции, проверка критически важного содержания, утверждение рукописи для публикации, Маркова Т.Н. — обзор публикаций по теме статьи, описание клинического случая, написание текста рукописи, редактирование.
Конфликт интересов: авторы заявляют об отсутствии возможных конфликтов интересов.
Анциферов Михаил Борисович — д. м. н., профессор, главный внештатный специалист-эндокринолог Департамента здравоохранения города Москвы, главный врач ГБУЗ «Эндокринологический диспансер ДЗМ». 119034, Россия, г. Москва, ул. Пречистенка, д. 37. eLIBRARY.RU SPIN: 1035-4773. https://orcid.org/0000-0002-9944-2997. E-mail: [email protected]
Маркова Татьяна Николаевна (автор для переписки) — д. м. н., доцент кафедры эндокринологии и диабетологии ФГБОУ ВО «МГМСУ им. А.И. Евдокимова» Минздрава России, заведующая эндокринологическим отделением ГБУЗ «ГКБ № 52 ДЗМ». 123182, Россия, г. Москва, ул. Пехотная, д. 3. eLIBRARY.RU SPIN: 5914-2890. https://orcid.org/0000-0002-8798-887X. E-mail: [email protected]
Ключевые слова: ожирение, медикаментозное лечение, индекс массы тела, лираглутидБольшинство ведущих мировых медицинских ассоциаций признали ожирение серьезной медико-социальной проблемой. Несмотря на высокий уровень образовательной активности, выпуск многочисленных публикаций по данной теме, как у врачей, так и у пациентов осталось немало вопросов, связанных с диагностикой, профилактикой и лечением ожирения. Когда же началась эпидемия ожирения? Многие считают, что эта проблема появилась в 80-х годах ХХ столетия. Однако еще 2500 лет назад Гиппократ предупреждал, что внезапная смерть чаще происходит у толстых от природы, чем у худых [1] . В 1760 году английский врач Малкольм Флеминг написал, что ожирение можно назвать болезнью, поскольку оно препятствует свободному осуществлению функций организма и может сократить продолжительность жизни [2] , а в 1810 году Уильям Вадд (секретарь Королевского колледжа хирургов в Лондоне) заявил, что рост благосостояния и утонченность современности, возможно, изгнали чуму и эпидемии, но привели к нервным расстройствам и увеличили распространенность полноты [3] . Лечение ожирения началось со времен Гиппократа, который рекомендовал таким пациентам изменить образ жизни [4, 5] . «Медикаментозная» терапия восходит к X веку, когда Хисдай ибн Шапрут вылечил Санчо Толстого от ожирения с помощью териака — смеси из более чем 64 ингредиентов [6] . Первые статьи по лечению ожирения были опубликованы в 1727 и 1760 годах и рекомендовали ромашковое мыло, уксус и другие растительные и природные средства [2, 7, 8] . В начале ХХ века в лечении ожирения начали использовать гормональные препараты и нейростимуляторы, такие как экстракт щитовидной железы, динитрофенол и амфетамин, которые приводили к тяжелым последствиям вплоть до смертельного исхода [9] . Открытие лептина в 1994 году (пептида, продуцируемого жировой тканью) знаменует начало «молекулярной эры» терапии ожирения. Лечение лептином дало прекрасные результаты у пациентов с генетически обусловленным дефицитом этого гормона, однако оказалось неэффективным у лиц с конституционально-экзогенным ожирением [10] . Прогресс фундаментальной науки середины и конца ХХ века ознаменовал новый этап понимания патогенеза экзогенно-конституционального ожирения. Нейрогуморальная дисфункция, которая клинически проявляется нарушением пищевого поведения, а также инсулинорезистентность с формированием висцерального ожирения являются основными звеньями патогенеза ожирения. Понимание механизмов регуляции приема пищи и массы тела дало надежду на разработку эффективных препаратов для терапии ожирения [11] . Однако существует немало препятствий для развития этой области фарминдустрии. До сих пор общество в целом, включая и медицинское сообщество, считает, что ожирение — результат отсутствия воли, распущенности [12] . Это приводит к тому, что пациенту предлагается изменить образ жизни, но не назначаются лекарственные препараты. Кроме того, желание пациента получить косметический эффект от потери массы часто намного превышает желание получить пользу для здоровья, связанную с уменьшением массы тела [13] . Это может объяснить тот факт, что женщин, обращающихся за помощью в борьбе с ожирением, больше, чем мужчин, несмотря на то что ожирение ассоциировано с кардиометаболическими заболеваниями независимо от пола человека [14] . Известно, что умеренная потеря массы (от 5% до 10%) уменьшает риск развития и прогрессирования заболеваний, ассоциированных с ожирением [15] , но такое снижение массы тела не дает ожидаемой пациентом косметической пользы. Это приводит к несоответствию между целями пациента и врача и уменьшает приверженность больных к лечению. В настоящее время наиболее распространенным методом оценки наличия и степени тяжести ожирения является расчет ИМТ по формуле: ИМТ = масса тела (кг)/рост (м 2 ). Большинство медицинских ассоциаций, а также Всемирная организация здравоохранения приняли ИМТ в качестве критерия диагноза ожирения. На сегодня последние клинические рекомендации Российской ассоциации эндокринологов по ожирению от 2020 г. также предлагают для диагностики ожирения использовать классификацию по уровню ИМТ. Нормальная масса тела определяется как ИМТ от 18,5 до 24,9 кг/м 2 , избыточная — от 25,0 до 29,9 кг/м 2 и ожирение ≥ 30 кг/м 2 [16] . Однако Американская ассоциация клинических эндокринологов (American Association of Clinical Endocrinology) предложила в 2014 г. использовать классификацию ожирения ( табл. 1 ) с учетом коморбидных заболеваний и диагностировать его при ИМТ ≥ 25 кг/м 2 , если имеется одно или несколько осложнений средней тяжести, связанных с ожирением [17] . Таблица 1
Классификация ожирения по стадиям с учетом коморбидных заболеваний (American Association of Clinical Endocrinology, 2014)
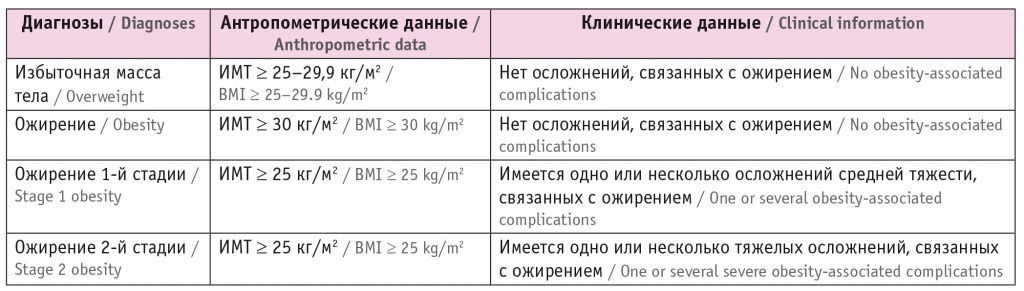
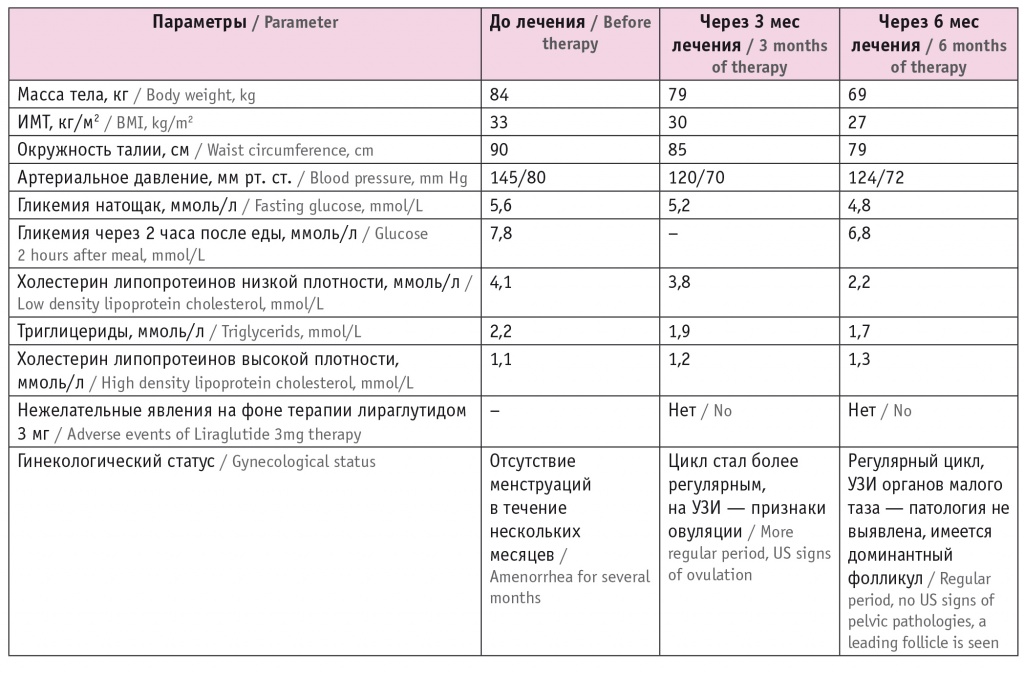
Примечание. Здесь и в таблице 2: ИМТ — индекс массы тела. Данная классификация предполагает, что для диагностики ожирения и верификации связанных с ним осложнений необходимо, помимо измерения антропометрических данных, провести клинические, инструментальные и лабораторные исследования. Патогенез коморбидности ожирения тесно связан с распределением жира в организме. Накопление висцерального или эктопического жира является одной из важнейших причин развития инсулинорезистентности, дислипидемии и других нарушений метаболического здоровья. Сейчас для диагностики абдоминального (висцерального) ожирения рекомендуется измерение окружности талии: ≥ 94 см у мужчин и ≥ 80 см у женщин — диагностический критерий абдоминального ожирения (International Diabetes Federation, 2005) [18] . Висцеральная жировая ткань синтезирует более 100 биологически активных веществ (адипоцитокинов) и становится источником хронического воспаления [19] . Кроме того, фермент ароматаза, который в больших количествах вырабатывает жировая ткань, метаболизирует андростендион в эстрон, что объясняет более высокий риск формирования рака молочной железы и эндометрия у женщин с ожирением, особенно в постменопаузе, поскольку эстрогены, синтезированные в жировой ткани, являются у них основными эстрогенами. Поэтому в настоящее время ряд онкологических заболеваний относят к патологиям, ассоциированным с ожирением [20] . У мужчин повышается риск рака кишечника и простаты, у женщин — рака молочных желез [21] , эндометрия [22] . Имеются неопровержимые доказательства того, что возрастание ИМТ, висцеральное ожирение и быстрые темпы увеличения массы тела способствуют развитию СД 2 типа (СД2), и ожирение является наиболее значимым модифицируемым фактором риска СД2 [23, 24] . Продолжительность ожирения, развитие его в молодом возрасте также связаны с более высоким риском СД2 [25] . Очевидно, что уменьшение массы тела способствует снижению этого риска. В Программе профилактики диабета средняя потеря веса на 5,5% в течение 2,8 года уменьшает риск перехода от предиабета к диабету на 58% [26] . С увеличением ИМТ и окружности талии увеличивается и риск сердечно-сосудистых заболеваний [27, 28] . Так, риск ИБС у женщин при ИМТ > 29 кг/м 2 в 3,3 раза выше, чем при ИМТ < 21 кг/м 2 [28] . В метаанализе 25 исследований выявлено, что потеря массы в среднем на 5,1 кг снижает АД на 4,4/3,5 мм рт. ст. (систолическое АД/диастолическое АД) [29] . Ожирение повышает риск формирования синдрома ночного апноэ во сне (СОАС) [30] . Патогенез и тяжесть СОАС у больных с ожирением связаны с выбросом факторов воспаления жировой тканью [31] . Исследование пациентов с ожирением с помощью полисомнографии показало, что 30,5% участников имели СОАС средней степени, а 22,6% — тяжелую форму. Окружность талии существенно влияла на наличие СОАС, а также на его тяжесть [32] . С ожирением ассоциируется также неалкогольная жировая болезнь печени, которая является одним из компонентов метаболического синдрома и может прогрессировать до неалкогольного стеатогепатита и, в итоге, до цирроза [33] . Нарушение репродуктивной функции как у мужчин, так и женщин тоже во многом обусловлено накоплением жировой ткани [34] . Лечение ожирения включает немедикаментозную и медикаментозную терапию и бариатрическую хирургию. В настоящее время оптимальным считают постепенное снижение массы тела (не более чем на 0,5–1 кг в неделю, 5–10% за 3–6 месяцев), направленное не столько на улучшение антропометрических показателей, сколько на компенсацию сопутствующих метаболических и гормональных нарушений. Важным аспектом эффективности лечения ожирения является поддержание эффекта в течение длительного времени (не менее 1 года) [16, 35] . Немедикаментозное лечение ожирения включает в себя диетотерапию (гипокалорийное питание с ограничением употребления жира до 25–30% от общей калорийности рациона), аэробные физические нагрузки (не менее 150 мин в неделю) и поведенческую терапию (терапевтическое обучение пациентов по структурированной программе и, при необходимости, консультацию психолога/психотерапевта) [16, 35, 36] . Назначение медикаментозной терапии ожирения рекомендовано при ИМТ ≥ 30 кг/м 2 или при ИМТ ≥ 27 кг/м 2 и наличии факторов риска и/или коморбидных заболеваний. В Российской Федерации для терапии ожирения зарегистрированы следующие препараты — орлистат, сибутрамин и лираглутид 3 мг [16, 36] . Орлистат — селективный ингибитор липазы поджелудочной железы, приводящий к снижению расщепления и всасывания жиров в кишечнике. В одном из клинических исследований масса тела снизилась на 9% за 1 год терапии против ~5,5% в группе плацебо [37] . В другом исследовании достигнуты снижение массы на 11% (в группе плацебо — лишь 6%) и уменьшение на 37% вероятности СД2 у больных с нарушенной толерантностью к глюкозе [38] . В метаанализе 31 исследования с использованием орлистата максимальная потеря массы (путем моделирования) составила 6,65 кг [39] . Однако приверженность к применению орлистата быстро снижается после первоначального назначения [40] , что связано с нежелательными явлениями, наблюдаемыми при приеме препарата, такими как жидкий маслянистый стул, вздутие и неконтролируемая дефекация, которые встречаются при превышении содержания жира в пище. Орлистат может уменьшать уровни жирорастворимых витаминов, поэтому пациентам, получающим орлистат, рекомендовано принимать дополнительно витамины D, A, E и K. Сообщалось о редких случаях тяжелого поражения печени у принимавших орлистат. Причинно-следственная связь не установлена, но больные, применяющие орлистат, должны связаться со своим лечащим врачом при появлении зуда, желтухи, бледного стула или анорексии [41] . Сибутрамин является ингибитором обратного захвата серотонина и норадреналина и действует на уровне ЦНС. Сибутрамин подавляет аппетит и увеличивает чувство насыщения, а также ускоряет энергетический обмен. Снижение массы на фоне терапии сибутрамином в исследовании STORM составило 10% [42] . Начальная доза сибутрамина составляет 10 мг. Рекомендуется увеличить дозу до 15 мг, если масса тела за первый месяц снизилась менее чем на 2 кг, при условии хорошей переносимости препарата. Если через 3 месяца приема сибутрамина масса тела снизилась менее чем на 5% от исходной, лечение считается неэффективным. Максимальный период терапии сибутрамином составляет 1 год. Помимо влияния на массу тела, сибутрамин оказывает благоприятное действие на метаболические показатели. Его применение сопровождается улучшением липидного профиля [42] . Наиболее частыми побочными явлениями при приеме сибутрамина являются повышение АД и учащение пульса. В связи с этим он не может быть назначен пациентам с неконтролируемой АГ, ИБС, декомпенсированной сердечной недостаточностью, нарушением ритма сердца и цереброваскулярными заболеваниями. При проведении терапии сибутрамином необходим монитринг АД и пульса. При учащении пульса более чем на 10 уд/мин, увеличении АД более чем на 10 мм рт. ст., а также в случае, если оно превышает 140/90 мм рт. ст. при ранее компенсированной АГ, сибутрамин отменяют. Исследование SCOUT [43] , посвященное изучению сердечно-сосудистых исходов при проведении долгосрочной терапии сибутрамином, в которое включены более 10 000 пациентов с ожирением или избыточной массой и отягощенным анамнезом в отношении сердечно-сосудистых заболеваний, было приостановлено досрочно в связи со значимым ростом частоты нефатального инфаркта миокарда и нефатального инсульта в группе сибутрамина. Риск сердечно-сосудистой смерти и смерти от всех причин в группе препарата не отличался от такового в группе плацебо. Результаты исследования SCAUT привели к отзыву препарата сибутрамина на территории Европейского союза и США [44] . Лираглутид является агонистом глюкагоноподобного пептида 1 типа (ГПП-1). ГПП-1 регулирует аппетит с помощью усиления чувства наполнения желудка и насыщения, одновременно ослабляя чувство голода и уменьшая предполагаемое потребление пищи за счет влияния на центры пищевого поведения. Молекула лираглутида на 97% гомологична нативному ГПП-1. За счет изменений структуры молекулы ГПП-1 период полувыведения лираглутида из циркулирующей крови увеличился с 1–2 минут до 13 часов. Лираглутид 3 мг показан в качестве средства длительной терапии в сочетании с низкокалорийной диетой и повышенной физической активностью взрослым пациентам с исходным ИМТ >30 кг/м 2 или при ИМТ от 27 кг/м 2 до > 30 кг/м 2 при наличии ассоциированных с ожирением заболеваний. Лираглутид противопоказан при наличии медуллярного рака щитовидной железы, беременности, тяжелой депрессии, тяжелых нарушениях функции печени и почек. Прием препарата прекращается при развитии острого панкреатита, о симптоматике которого должен быть предупрежден пациент. Если к 16 неделям терапии потеря массы не превышает 5%, она считается неэффективной, и больной должен прекратить прием лираглутида 3 мг. Исследование второй фазы, в котором анализировались эффективность и безопасность лираглутида в дозах 1,2, 1,8, 2,4 и 3 мг, продемонстрировало снижение массы на 3,8, 5,4, 6,1 и 7,8 кг соответственно через 1 год лечения против 2 кг в группе плацебо и 3,9 кг в группе орлистата [45] . Таким образом, доза 3 мг оказалась более эффективной, чем другие дозы лираглутида и орлистат. В более крупном исследовании «SCALE, ожирение и предиабет» через 56 недель лираглутид 3 мг снизил массу тела на 8,4 кг против 2,8 кг в группе плацебо. Лираглутид 3 мг также продемонстрировал позитивное влияние на АД, показатели липидного профиля и маркеры сердечно-сосудистого риска [46] . В исследовании «SCALE поддержание» пациенты, получавшие лираглутид после первоначального снижения массы с помощью низкокалорийной диеты, потеряли дополнительно 6,8 кг в отличие от больных из группы плацебо, в которой наблюдалось увеличение массы тела. При этом суммарное снижение массы тела в группе лираглутида 3 мг составило 12,2 кг за 56 недель [47] . Продление наблюдения за пациентами с предиабетом до 3 лет продемонстрировало уменьшение риска СД2 на 80%. Таким образом, лираглутид 3 мг не только способствовал уменьшению массы тела, но и позитивно влиял на факторы сердечно-сосудистого риска и гликемический профиль [48] . Представляют интерес результаты медикаментозной терапии ожирения в клинической практике. В литературе описано немало случаев успешного лечения морбидного ожирения. Однако терапия начальных стадий заболевания особенно важна для обратного развития ассоциированных патологий и профилактики тяжелых осложнений. Вашему вниманию предлагается история болезни пациентки 30 лет, обратившейся с жалобами на постепенную прибавку массы тела, не поддающуюся коррекции изменением образа жизни. В 18 лет ее масса составляла 60 кг, на момент осмотра — 84 кг, прибавка произошла постепенно (2–3 кг в год). Неоднократно худела, соблюдая различные диеты, но удержать достигнутый результат не удавалось. Приемы пищи 2 раза в день (завтрак, поздний ужин), имела нарушения пищевого поведения: «заедание» стрессов, синдром ночной еды, пищевые «кутежи» (за один прием может употребить до 2000 ккал). Физическая активность минимальная, офисная работа. В 25 лет диагностирован синдром поликистозных яичников (СПКЯ), больная получала гормональную терапию 6 мес. На момент осмотра у женщины отсутствовали менструации в течение 6 мес. Планировала беременность, в связи с чем обратилась к эндокринологу. Имеет отягощенную наследственность: у матери ожирение 1-й степени и СД2. С 27 лет отмечала повышение АД (с 29 лет постоянно получала периндоприл). При объективном осмотре: рост — 160 см, масса — 84 кг, ИМТ — 33 кг/м 2 , избыточный рост волос по белой линии живота и внутренней поверхности бедер, абдоминальный тип распределения подкожно-жировой клетчатки, окружность талии — 90 см. АД — 145/80 мм рт. ст., ЧCC — 72 уд/мин. По результатам биохимического и гормонального исследования у пациентки диагностировали гиперурикемию, нарушенную толерантность к глюкозе (по данным перорального глюкозотолерантного теста), дислипидемию в виде снижения уровня ЛПВП. На основании вышеизложенного выставлен следующий диагноз: Ожирение 1-й степени, экзогенно-конституциональное. Нарушенная толерантность к глюкозе. Дислипидемия. Синдром поликистозных яичников. Пациентке назначена программа по коррекции массы с целевыми показателями по снижению массы тела на 10% за 6 месяцев. Программа включала гипокалорийное питание (1400 ккал с ограничением легкоусвояемых углеводов, жиров до 40 г в день), ежедневную аэробную физическую нагрузку по 30 мин в день в сочетании с умеренной силовой нагрузкой 2–3 раза в неделю. С учетом ИМТ более 27 кг/м 2 , наличия ассоциированных с ожирением заболеваний (СПКЯ, АГ, гиперурикемии и дислипидемии) назначена медикаментозная терапия — лираглутид 3 мг (Саксенда) подкожно 1 раз в день не менее 6 месяцев с титрацией дозы при старте терапии по 0,6 мг в неделю до достижения 3 мг. Динамика физикального статуса и результаты лабораторно-инструментального обследования представлены в таблице 2 . Таблица 2
Динамика изучаемых параметров у пациентки на фоне лечения лираглутидом 3 мг

Таким образом, в результате лечения пациентка снизила массу тела на 15 кг за 6 месяцев, что составляет 18% от первоначальной массы тела, ИМТ уменьшился с 33 кг/м 2 (1-я степень ожирения) до 27 кг/м 2 (избыточная масса тела), окружность талии — с 90 см до 79 см, что соответствует низкому сердечно-сосудистому риску: достигнуты ремиссия предиабета и улучшение показателей липидного спектра. Нормализовался менструальный цикл, а также появились признаки овуляторной активности при проведении УЗИ яичников. ЗАКЛЮЧЕНИЕ Ожирение — это хроническое заболевание, характеризующееся избыточным накоплением жировой ткани в организме, представляющим угрозу здоровью. Оно также является основным фактором риска ряда других хронических болезней, в том числе СД 2 типа и сердечно-сосудистых заболеваний, лимитирующих продолжительность жизни больных. Следовательно, пациенты с ожирением и избыточной массой тела должны обязательно обследоваться у врача с целью верификации ассоциированных заболеваний и назначения лечения, включая медикаментозную терапию, направленную на снижение массы тела. Поступила: 25.01.2021
Принята к публикации: 11.03.2021




