Диссертация на тему «Сравнительное исследование результатов эндоваскулярного лечения больных с различными типами клинического течения артериовенозных мальформаций головного мозга», скачать бесплатно автореферат по специальности ВАК РФ 14.01.18 - Нейрохиру
Сравнительное исследование результатов эндоваскулярного лечения больных с различными типами клинического течения артериовенозных мальформаций головного мозга тема диссертации и автореферата по ВАК РФ 14.01.18, кандидат наук Брусянская Анна Сергеевна
Оглавление диссертации кандидат наук Брусянская Анна Сергеевна
ГЛАВА 1 ОБЗОР ЛИТЕРАТУРЫ
1.1 Определение артериовенозных мальформаций
1.2 Эпидемиология артериовенозных мальформаций
1.3 Морфология артериовенозных мальформаций
1.4 Клинические типы течения артериовенозных мальформаций
1.5 Классификация артериовенозных мальформаций по степени хирургического риска
1.6 Эпилепсия при церебральных артериовенозных мальформациях
1.7 Методы, используемые в лечении пациентов с артериовенозными мальформациями головного мозга
1.8 Полученные результаты в этой области нейрохирургии на сегодняшний день
1.9 Какие остаются проблемы в лечении структурной эпилепсии у больных с
артериовенозными мальформациями головного мозга
ГЛАВА 2 МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
2.1 Дизайн исследования
2.2 Методы обследования и ведения больных
2.3 Методы лечения
2.4 Эмболизирующие материалы, используемые в исследовании
2.5 Этапы клинического исследования
2.6 Статистический анализ данных
ГЛАВА 3 РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
3.1 Характеристика больных с эпилептическим типом течения артериовенозных мальформаций
3.2 Общая характеристика больных с эпилептическим и геморрагическим типом течения. До Propensity Score Matching
3.3 Общая характеристика больных с эпилептическим и геморрагическим типом течения. После Propensity Score Matching
3.4 Результаты лечения общей когорты эпилептической группы больных с артериовенозными мальформациями головного мозга (основные исходы) в периоперационном периоде
3.4.1 Исходы интраоперационного периода в эпилептической группе
3.4.2 Осложнения, возникшие в первые трое суток после оперативного лечения в обеих группах больных с эпилептическим типом течения артериовенозных мальформаций головного мозга
3.4.3 Отдаленные результаты лечения группы с эпилептическим типом течения
3.5 Сравнительный анализ групп (отобранных методом Propensity Score
Matching) с эпилептическим и геморрагическим типом течения
3.5.1 Исходы интраоперационного периода в обеих группах
3.5 2 Ранние послеоперационные осложнения (первые трое суток после операции) в обеих группах
3.6 Сравнение полученных результатов исследования с естественным течением артериовенозных мальформаций головного мозга
3.6.1 Сравнение данных естественного течения артериовенозных мальформаций головного мозга с полученными данными исследования в отношении рисков кровоизлияния, инвалидизации и летальности
3.6.2 Сравнение лечения фармакорезистентной эпилепсии с помощью противоэпилептических препаратов и методом эндоваскулярной эмболизации
3.6.3 Сравнение результатов после тотальной и парциальной эмболизации в отношении свободы от приступов
3.7 Клинические примеры
СПИСОК СОКРАЩЕНИЙ И УСЛОВНЫХ ОБОЗНАЧЕНИЙ
СПИСОК ИЛЛЮСТРАТИВНОГО МАТЕРИАЛА
Артериовенозные мальформации (АВМ) головного мозга являются врожденной патологией сосудов и представляют собой клубок переплетенных сосудов (артерий, вен), не имеющих капиллярной сети. Распространенность церебральных АВМ по разным источникам варьирует от 0,8 до 1,42 на 100 тыс. населения в год [3, 85].
Выделяют два основных варианта клинического течения АВМ головного мозга: торпидный и геморрагический. Торпидный, или псевдотуморозный, тип течения АВМ характеризуется дебютом судорожного синдрома, кластерных головных болей, симптоматики прогрессирующего неврологического дефицита. Чаще всего наблюдаются судорожные припадки (до 67 % всех больных с АВМ) [27], которые у 87,9 % больных дебютируют до 30-летнего возраста. Простые парциальные припадки наблюдаются у 10 %, сложные парциальные - у 4,3 %, парциальные с вторичной генерализацией - у 22,4 %, генерализованные - у 63,3 % больных [25]. Из других симптомов отмечаются прогрессивные неврологические нарушения (19,6 %), головная боль и головокружение (11,8 %). В 27,5 % наблюдений торпидное течение заболевания осложняется кровоизлияниями, которые обусловливают последующее развитие судорожного синдрома у 18 % больных [25]. Геморрагический тип течения отмечается в 30-87 % наблюдений всех АВМ, преимущественно характерен для категорий I—III по Spetzler - Martin (SM) [114, 85]. АВМ головного мозга диагностируют в основном у пациентов в возрасте от 30 до 40 лет и только у 18-20 % - до 15 лет. Обнаружение АВМ в детском возрасте считают более опасным, чем у взрослых, поскольку в период от 15 до 40 лет риск разрыва АВМ наибольший и достигает 80 % [3].
На сегодняшний день для лечения больных с артериовенозными мальформациями применяют следующие методы: симптоматическая терапия, эндоваскулярный (эмболизация), микрохирургический (удаление мальформации)
Все методы хирургического лечения направлены на тотальное выключение мальформации из кровотока, с целью исключения риска кровоизлияния, ликвидации феномена обкрадывания мозга, снижения или регресса неврологического дефицита, а также с целью контроля эпилептических приступов при наличии структурной эпилепсии. По опубликованным данным многих авторов наиболее эффективным в отношении тотального выключения АВМ является микрохирургическое лечение. Однако не все АВМ доступны для микрохирургического удаления, в особенности это касается крупных и гигантских АВМ IV-V градации по Spetzler - Martin. В связи с этим многим пациентам проводится эндоваскулярное этапное лечение или комбинированное вмешательство (эндоваскулярное выключение доступных афферентов с последующим микрохирургическим или радиохирургическим выключением). Показания к хирургическому лечению мальформаций при геморрагическом типе не вызывают сомнения. Однако тактика лечения больных с АВМ головного мозга при торпидном типе течения окончательно не определена. Международное многоцентровое рандомизированное исследование ARUBA [28] показало, что на протяжении 33 месяцев наблюдения медикаментозное лечение имеет преимущество перед интервенционным (микрохирургия, эндоваскулярная эмболизация, радиохирургия) для предупреждения смерти от инсульта у больных с неразорвавшимися АВМ. Дальнейшее наблюдение за этими больными продолжается. Тем не менее, открытым остается вопрос тактики ведения больных с АВМ, страдающих структурной эпилепсией при неэффективности медикаментозного лечения и более высоком риске развития кровоизлияния при развитии эпиприступа. Хотя отсутствие лечения в данной группе пациентов приводит к значительному снижению качества их жизни, на настоящий момент нет исследований больших групп пациентов с эпилептическим типом течения АВМ головного мозга, которые бы показывали, что хирургическое лечение не ухудшает их состояние [82, 109, 127]. Проведение рандомизированного
исследования, сравнивающего хирургическое лечение с его отсутствием не представляется возможным по этическим причинам. Однако, есть возможность оценить эффективность лечения по динамике клинических проявлений, а также оценить безопасность эндоваскулярного лечения в группе пациентов с эпилептическим типом течения, по сравнению с группой пациентов с геморрагическим типом течения, для оценки рисков и возможных преимуществ вмешательства.
Оценить эффективность и безопасность эндоваскулярного лечения у больных с геморрагическим и эпилептическим типами клинического течения артериовенозных мальформаций головного мозга с учётом динамики клинических проявлений и частоты развития интра- и послеоперационных осложнений.
1. Сравнить частоту интраоперационных и ранних послеоперационных осложнений у больных с геморрагическим и эпилептическим типами течения артериовенозных мальформаций головного мозга после проведения им эндоваскулярной эмболизации.
2. Оценить динамику неврологического статуса у оперированных больных методом эндоваскулярной эмболизации с геморрагическим и эпилептическим типом течения артериовенозных мальформаций головного мозга по шкале Рэнкина (the Modified Rankin Scale (mRS) в сравнении с исходными данными.
3. Сравнить динамику эпилептических приступов у больных с эпилептическим типом течения артериовенозных мальформаций головного мозга с помощью шкал Engel и ILAE после выполнения им парциальной и тотальной эмболизации.
4. Определить степень рисков кровоизлияний, инвалидизации и смертности в группе с эпилептическим типом течения артериовенозных
мальформаций головного мозга после выполнениям им этапной эмболизации мальформации в сравнении с естественными рисками данного заболевания.
5. Сравнить эффективность применения противосудорожной терапии и её сочетания с эндоваскулярной эмболизацией в отношении свободы от приступов у больных со структурной фармакорезистентной эпилепсией при артериовенозных мальформациях головного мозга.
Практическая значимость работы заключается в том, что:
- эндоваскулярное лечение пациентов с эпилептическим типом течения АВМ является безопасным и эффективным методом лечения структурной эпилепсии и приводит к улучшению качества жизни пациентов.
- этапная эмболизация не усугубляет состояние пациента по результатам оценки по шкале Рэнкина.
- с помощью шкал исходов хирургического лечения Engel и ILAE доказано улучшение течения структурной эпилепсии даже при парциальном выключении АВМ.
Положения, выносимые на защиту:
1. Этапная эмболизация артериовенозной мальформации головного мозга положительно влияет на течение структурной эпилепсии у данной группы больных, увеличивая контроль над эпилептическими приступами и улучшая качество жизни пациентов, при этом эндоваскулярная эмболизация дает лучший контроль над эпилептическими приступами у больных со структурной эпилепсией при артериовенозной мальформации головного мозга, чем правильно подобранные противоэпилептические препараты у пациентов с фармакорезистентной эпилепсией.
2. Эндоваскулярная эмболизация не превышает естественные риски течения артериовенозной мальформации головного мозга с эпилептическим типом в отношении развития тяжелой инвалидизации и летальности, что позволяет рекомендовать данный метод в лечении этих пациентов. Кроме того, риски интра- и послеоперационных осложнений у пациентов с геморрагическим
типом течения артериовенозной мальформации головного мозга выше, чем у пациентов с эпилептическим типом течения, что подтверждает необходимость хирургического лечения пациентов с кровоизлиянием вследствие разрыва артериовенозной мальформации головного мозга в анамнезе.
Рекомендованный список диссертаций по специальности «Нейрохирургия», 14.01.18 шифр ВАК
КОМБИНИРОВАННОЕ ЛЕЧЕНИЕ ДЕТЕЙ С ЦЕРЕБРАЛЬНЫМИ АРТЕРИОВЕНОЗНЫМИ МАЛЬФОРМАЦИЯМИ, СОПРОВОЖДАЮЩИМИСЯ ЭПИЛЕПТИЧЕСКИМИ ПРИСТУПАМИ 2016 год, кандидат наук Тадевосян Арсен Рустамович
Артериовенозные мальформации головного мозга супратенториальной локализации у детей (клиника, диагностика, хирургическое лечение) 2011 год, кандидат медицинских наук Краснова, Мария Александровна
РЕЗУЛЬТАТЫ ЭНДОВАСКУЛЯРНОГО ЛЕЧЕНИЯ АРТЕРИОВЕНОЗНЫХ МАЛЬФОРМАЦИЙ ГОЛОВНОГО МОЗГА С ПРИМЕНЕНИЕМ КОМБИНАЦИИ СУПЕРАБСОРБИРУЮЩИХ МИКРОСФЕР (HEPASPHERE) И ГИСТОАКРИЛА (NBCA) 2013 год, кандидат медицинских наук ГАФУРОВ, РУСТАМ РАСИМОВИЧ
Микрохирургическое лечение неразорвавшихся АВМ головного мозга: оценка результатов, уточнение показаний 2020 год, кандидат наук Горожанин Вадим Александрович
Микрохирургическое иссечение артериовенозных мальформаций головного мозга с предварительной эндоваскулярной эмболизацией 2023 год, кандидат наук Дмитриев Алексей Вячеславович
Введение диссертации (часть автореферата) на тему «Сравнительное исследование результатов эндоваскулярного лечения больных с различными типами клинического течения артериовенозных мальформаций головного мозга»
Материалы диссертации доложены и обсуждены на: 1-м и 2-м Сибирском нейрохирургическом конгрессе «Сибнейро» (Новосибирск, 2016, 2018), 16-м конгрессе Международного Общества нейрохирургов (WFNS World Congress of Neurosurgery) (Стамбул, 2017), 8-м Российском нейрохирургическом конгрессе (Санкт-Петербург, 2018), ежегодной научной встрече американской ассоциации нейрохирургов (AANS) (Новый Орлеан, 2018), на ежегодной встрече общества нейроинтервенциональных хирургов (SNIS) (Сан-Франциско, 2018), 46-м международном детском нейрохирургическом конгрессе (Тель-Авив, 2018). Диссертационная работа апробирована на заседании проблемной комиссии «Актуальные проблемы хирургических методов лечения заболеваний» ФГБОУ ВО «Новосибирский государственный медицинский университет» Минздрава России (Новосибирск, 2019).
Диссертационная работа выполнена в соответствии с утвержденным направлением научно-исследовательской работы ФГБОУ ВО «Новосибирский государственный медицинский университет» Минздрава России по теме: «Разработка и совершенствование методов профилактики, раннего выявления и хирургического лечения повреждений и заболеваний органов грудной и брюшной полости, органов головы, шеи и опорно-двигательного аппарата», номер государственной регистрации АААА-А15-115120910167-4.
Публикации и сведения о внедрении в практику
По материалам диссертации опубликовано 13 научных работ, в том числе 4 статьи в научных журналах и изданиях, которые включены в перечень рецензируемых научных изданий, в которых должны быть опубликованы основные научные результаты диссертаций на соискание ученой степени
кандидата наук, на соискание ученой степени доктора наук, из них 1 статья в журнале, входящем в международную реферативную базу данных и систем цитирования (Scopus).
1. Контроль эпилептических приступов у больных с артериовенозными мальформациями после эндоваскулярного лечения / А. Л. Кривошапкин [и др., в том числе А. С. Брусянская] // Нейрохирургия. - 2017. - № 3. - C. 27-33.
2. Результаты инвазивного лечения больных с эпилептическим типом течения артериовенозных мальформаций головного мозга / А. Л. Кривошапкин [и др., в том числе А. С. Брусянская] // Сибирский Научный Медицинский Журнал. -2018. - Том 38, № 6. - С. 145-153.
3. Сравнение результатов эндоваскулярной эмболизации у больных с геморрагическим и эпилептическим типом течения артериовенозных мальформаций головного мозга / А. С. Брусянская [и др.] // Вестник неврологии, психиатрии и нейрохирургии. - 2019. - № 5 (112). - С. 70-76.
4. Сравнение результатов и выявление предикторов неблагоприятного исхода после эндоваскулярной эмболизации у больных с разными типами течения артериовенозных мальформаций головного мозга / А. С. Брусянская [и др.] // Патология кровообращения и кардиохирургия. - 2019. - № 23 (1). - С. 54-60.
Результаты исследования внедрены в практическую деятельность нейрохирургического отделения ФГБУ «НМИЦ им. акад. Е.Н. Мешалкина» Минздрава России, а также в учебный процесс клинических ординаторов и аспирантов, обучающихся на базе ФГБУ «НМИЦ им. ак. Е.Н. Мешалкина» Минздрава России и кафедры нейрохирургии ФГБОУ ВО «Новосибирский государственный медицинский университет» Минздрава России.
Внедрение результатов исследования
Полученные в данном исследовании результаты в настоящее время используются как практические рекомендации в протоколах ведения больных с артериовенозными мальформациями головного мозга в центре нейрохирургии и ангионеврологии ФГБУ «НМИЦ им. ак. Е. Н. Мешалкина» Минздрава России.
Данные протоколы ведения больных с АВМ головного мозга и с разными типами течения входят в программу обучения клинических ординаторов и аспирантов, обучающихся на базе ФГБУ «НМИЦ им. ак. Е.Н. Мешалкина» Минздрава России и кафедры нейрохирургии ФГБОУ ВО «Новосибирский государственный медицинский университет» Минздрава России.
В дальнейшем результаты нашего исследования, возможно, будут применены в общероссийские алгоритмы лечения больных с АВМ и с разными типами течения.
Объем и структура работы
Диссертация изложена на 143 страницах машинописного текста и состоит из введения, 3 глав, заключения, выводов, практических рекомендаций, списка сокращений и условных обозначений, списка литературы и списка иллюстративного материала. Список литературы представлен 132 источниками, из которых 106 в зарубежных изданиях. Полученные результаты проиллюстрированы с помощью 21 таблицы и 37 рисунков.
Личный вклад автора в работу
Автором выполнено клиническое исследование пациентов, проведён анализ эпилептических приступов в соответствии со шкалами Engel и ILAE, с последующей аналитической обработкой и статистическим анализом полученных данных, сформулированы выводы и практические рекомендации. Автором проанализированы основные отечественные и зарубежные литературные данные, подготовлены публикации по теме диссертационной работы.
ГЛАВА 1. ОБЗОР ЛИТЕРАТУРЫ
1.1 Определение артериовенозных мальформаций
Артериовенозные мальформации (АВМ) головного мозга представляют собой порок развития церебральных артерий, характеризующийся образованием патологического скопления кровеносных сосудов, через которые артериальная кровь попадает непосредственно в дренирующие вены, не проходя через нормальное капиллярное русло. Внутри узла мозговое вещество отсутствует. Артериовенозные мальформации являются врожденными поражениями, которые имеют тенденцию к увеличению в течение жизни. Часто при рождении кровоток в этих образованиях низкий, но затем у взрослых он возрастает до средневысокого, а давление в них увеличивается. Макроскопически АВМ имеют вид клубка сосудов, часто с хорошо отграниченным центральным узлом и дренажными «красными» венами (содержат оксигенированную кровь) [46, 63]. Артериовенозные мальформации головного мозга возникают в результате внутриутробных локальных нарушений формирования церебральной сосудистой сети. Причинами таких нарушений являются различные вредоносные факторы, влияющие на плод в течение антенатального периода: повышенный радиоактивный фон, внутриутробные инфекции, заболевания беременной (сахарный диабет, хронический гломерулонефрит, бронхиальная астма и др.), интоксикации, вредные привычки беременной (наркомания, курение, алкоголизм), прием во время беременности фармакологических препаратов, имеющих тератогенный эффект. Возможно, существует генетическая предрасположенность к этой патологии, так как дефект может наблюдаться одновременно у нескольких представителей семьи, принадлежащих к разным поколениям, при этом «наследственные» мальформации чаще всего встречаются у мужчин [131].
Церебральные артериовенозные мальформации могут располагаться в
любом месте головного мозга: как на его поверхности, так и в глубине: в супратенториальных структурах локализуются около 86 % всех АВМ (в области мозгового плаща - 47 %, лимбической системы - 9 %, глубинных структур -30 %), субтенториальных - 14 % (мозжечка - 12 %, ствола - 2 %) [128].
Сегодня большое количество научных статей посвящено предикторам развития внутричерепных кровоизлияний вследствие разрыва АВМ головного мозга. Таковыми считаются наличие глубокого венозного дренажа и диффузного клубка мальформации, аневризмы внутри клубка мальформации, множественные аневризмы, расположение АВМ в области кровоснабжения вертебро-базилярного бассейна и подкорковых ядер [49].
В 1979 г. принята международная гистологическая классификация опухолей ЦНС ВОЗ, в которой АВМ относятся к группе сосудистых мальформаций.
Последняя отечественная классификация сосудистых пороков развития разработана Д. Е. Мацко (1993 г.):
1) ангиоматозные пороки развития:
а) в пределах ЦНС,
б) факоматозы (болезнь Стерджа-Вебера, синдром Клиппель-Треноне, и др.),
2) неангиоматозные пороки развития:
- артериовенозные (синусные) фистулы и соустья,
- персистирующие эмбриональные сосуды,
- другие неангиоматозные пороки развития,
3) неклассифицируемые пороки развития.
Наиболее подробную топографо-анатомическую классификацию, отражающую локализацию, кровоснабжение и дренажи, эмбриогенетическое происхождение АВМ предложил A. Valavanis (1996) [128].
Супратенториальные артериовенозные мальформации (86 % всех АВМ головного мозга):
1) неопаллиальные артериовенозные мальформации (47 %) (лобная, височная, теменная, затылочная и центральная):
а) сулькарная (собственно в борозде, с извилиной, с паравентрикулярным распространением),
б) гиральная (собственно в извилине, под извилиной, с паравентрикулярным распространением),
в) сочетание гиральной с сулькарной (под извилиной, с паравентрикулярным распространением),
2) архи- и палеопаллиальные артериовенозные мальформации (9 %) (в т. ч. лимбическая и паралимбическая артериовенозная мальформация: поясная, гипо-парагипокампальная, септальная, инсулярная артериовенозные мальформации):
б) гиральная, паренхимальная,
г) желудочковая (височный рог),
3) глубинные центральные артериовенозные мальформации (27 %) (стриоталамокапсулярные, диэнцефальные, мезэнцефальные и сосудистое сплетение желудочков):
a) фиссуральные, цистернальные,
г) сосудистое сплетение желудочков (боковой и/или III желудочек),
4) аневризматическая мальформация вены Galen (3 %).
Инфратенториальные артериовенозные мальформации (14 %):
1) неоцеребеллярные артериовенозные мальформации (11 %):
а) сулькарная, фиссуральные,
2) палео- и архицеребеллярные артериовенозные мальформации (1 %):
а) сулькарная, гиральная,
3) глубинно-центральные артериовенозные мальформации (2 %) (ядра мозжечка, ствол мозга, внутрижелудочковая артериовенозная мальформация):
а) сулькарная, цистернальная,
в) внутрижелудочковая (IV желудочек и/или водопровод).
1.2 Эпидемиология артериовенозных мальформаций
По результатам эпидемиологических исследований известно, что распространённость данного заболевания составляет 0,8-1,42 случаев на 100 тыс. населения [3, 85]. По данным литературы соотношение мужчин и женщин в среднем колеблется 1,4 : 1 [92]. Такие аномалии могут оказаться фатальными, поскольку высокий артериальный поток может нарушить целостность венозных стенок, что приводит к опасным последствиям, таким как кровоизлияние.
Отдаленный прогноз при консервативном лечении АВМ головного мозга неблагоприятен: глубокая инвалидизация наступает у 48 % носителей АВМ,
а 23 % больных погибают [31]. Выживаемость больных АВМ оставляет 85 % в первые 10 лет, 65 % в течение 30 лет с момента установления диагноза [125]. Активная лечебная тактика способствует снижению ежегодной смертности с 3,4 % при консервативном лечении до 1,2 % при радикальном вмешательстве [30, 86].
1.3 Морфология артериовенозных мальформаций
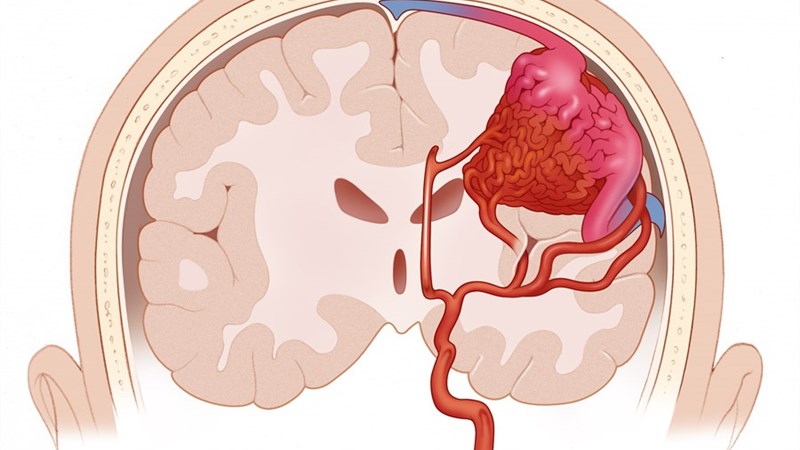
Типичные АВМ представлены тремя основными компонентами: приводящими артериями (афференты АВМ), клубком измененных сосудов (ядро) мальформации, дренирующими венами (эфференты АВМ) (рисунок 1).
Рисунок 1 - Типичная морфология АВМ головного мозга (данные церебральной ангиографии)
Для приводящих сосудов наиболее характерным является более или менее выраженное расширение просвета и удлинение, следствием чего является патологическая извитость и деформация магистральных артерий шеи, магистральных внутричерепных сосудов. Увеличение калибра артерии является следствием патологического возрастания объемного кровотока и линейной
скорости кровотока в афферентном сосуде. Нередко калибр артерии увеличивается в дистальных сегментах, непосредственно перед входом в клубок мальформации. Объем клубка мальформации косвенно определяет выраженность шунтирования и степень расширения питающих артерий. По степени участия в кровоснабжении АВМ питающие артерии могут быть как «концевыми» (кровь попадает только в мальформацию), так и «транзитными» (отдавая ветви к мальформации, артерия преимущественно участвует в кровоснабжении мозга). Количество питающих артерий может быть различным: от одной (при мелких АВМ) до нескольких (при АВМ среднего и крупного размера). При обследовании следует четко определить источники кровоснабжения АВМ, прежде всего, дифференцировать поверхностные (ветви корковых ветвей мозговых артерий) и глубинные (ветви лентикулостриарных, перфорантных и ворсинчатых артерий) афференты. Ликвидация глубинных источников кровоснабжения АВМ представляет наибольшие сложности, как при микрохирургических, так и внутрисосудистых вмешательствах, несет максимальный риск кровотечения и ишемических осложнений. Ядро мальформации представляет собой клубок переплетенных сосудов различного калибра (от 100 до 3 000 мкм), являющихся прямыми артериовенозными анастомозами без микроциркуляторного русла. Клубок АВМ может иметь форму шара, пирамиды или усеченной пирамиды, двояковыпуклой линзы, цилиндра. Ядро может располагаться как в субарахноидальном пространстве, так и в паренхиме мозга, паравентрикулярно. В стенках сосудов АВМ отмечается уплотнение и пролиферация интимы, внутренняя эластическая мембрана подвергается дегенеративным изменениям. Большинство сосудов неравномерно расширены и изменены настолько, что определить их принадлежность к артериям или венам невозможно. В ряде случаев сосудистая стенка построена из соединительной ткани и напоминает стенку аневризм. Нередки интрамуральные петрификаты. В сосудах с уплотненной стенкой, нередко гиалинизированной, может выявляться амилоид. В просвете часто обнаруживаются пристеночные и реканализированные тромбы. Описаны
три основных анатомических варианта строения ядра АВМ [62]: фистульный (артерия непосредственно переходит в вену, как правило, с выраженной эктазией переходного участка) - 11 %, плексиформный (связь артерий с венами осуществляется через клубок диспластических сосудов) - 36 %, смешанный (сочетание фистульного варианта с плексиформным) - 53 %. В участках мозга, окружающих и заключенных между сосудистыми петлями АВМ отмечаются выраженные дистрофические изменения, что является реакцией мозговой ткани на травмирующие пульсовые воздействия, кровоизлияния, хроническую недостаточность кровоснабжения. Из клубка АВМ исходят аномально расширенные извитые вены. Нередко отмечается как локальное расширение вен -варикс, так и сужение - стеноз. При крупных мальформациях часто наблюдается выраженная асимметрия строения (и венозного оттока из полости черепа) крупных синусов, в частности поперечного, который на стороне мальформации бывает сужен, в связи с чем нагрузка ложится преимущественно на яремную вену здоровой стороны, что обуславливает затруднение венозного оттока из полости черепа. Дренирование артериальной крови из клубка АВМ может осуществляться как в систему поверхностных корковых вен, так и в систему «глубоких» вен мозга со стоком в вену Галена. При крупных АВМ конвекситальной и базальной поверхности мозга участие в их кровоснабжении могут принимать ветви наружной сонной артерии, как правило, через оболочечные артерии. Особенно велико участие в кровоснабжении ветвей наружной сонной артерии при АВМ, расположенных вблизи крупных синусов твердой мозговой оболочки. Локализация АВМ неспецифична и пропорциональна объему отдела головного мозга: в супратенториальных структурах локализуются около 86 % всех АВМ (в области мозгового плаща - 47 %, лимбической системы - 9 %, глубинных структур - 30 %), субтенториальных - 14 % (мозжечка - 12 %, ствола - 2 %) [33, 48, 94].
1.4 Клинические типы течения артериовенозных мальформаций
Артериовенозные мальформации головного мозга являются врожденной аномалией развития церебрального русла.
Клинические типы течения АВМ, как правило, представлены двумя типами: геморрагическим (42 % - 72 %) и торпидным (20 % - 67 %) [27, 114]. В значительно меньшем проценте случаев АВМ головного мозга могут проявляться неспецифическими симптомами, такие как головные боли, шум в голове, прогрессирующий неврологический дефицит или АВМ является находкой по данным нейровизуализации (от 5 % до 15 % случаев) [40, 84, 109]. Артериовенозные мальформации головного мозга могут проявляться в любом возрасте. Однако в детской практике мальформации головного мозга преимущественно проявляются развитием внутричерепного кровоизлияния и данный тип течения у детей достигает 87,5 % по данным литературы [52, 79, 109]. Во взрослой когорте больных с артериовенозными мальформациями головного мозга геморрагический тип течения также встречается чаще, чем торпидное течение, однако частота развития внутричерепного кровоизлияния варьирует от 42 % до 72 %, по мнению ряда авторов [68, 97].
Геморрагический тип. Кровоизлияние является самым опасным проявлением АВМ, в связи с чем лечение мальформаций, преимущественно, направлено на предотвращение кровоизлияний. Геморрагический тип течения, преимущественно, характерен для мальформаций I-III градации по Spetzler - Martin, что объясняется более высоким давлением в питающих артериях малых АВМ, по сравнению с более крупными [25]. Риск кровотечения вследствие разрыва АВМ составляет 2,10-4,12 % в год [52, 85]. Кроме того, по данным литературы, риск разрыва неразорвавшихся АВМ в течение 10 и 20 лет составляет 16 % и 29 %, соответственно, а разорвавшихся АВМ 35 % и 45 % через 10 и 20 лет, соответственно [43, 65]. На сегодняшний день, учитывая факторы предикторы (такие как наличие аневризм в составе клубка АВМ (интранидальные аневризмы), глубинная локализация АВМ, малый размер АВМ), выделяются
четыре группы больных АВМ по степени риска кровоизлияния: I (низкого риска) - 0,99 % в год, II (относительно низкого риска) - 2,22 % в год, III (относительно высокого риска) - 3,72 % в год, IV (высокого риска) - 8,94 % в год [21, 45,73]. Риск хирургического лечения оценивается по специальной шкале Spetzler - Martin (SM). Эта шкала учитывает ряд характеристик АВМ, важных для хирургического лечения. Размер учитывается за счет присвоения 1 балла для АВМ менее 3 см в диаметре, 2 баллов для АВМ от 3 до 6 см, и 3 баллов для АВМ более 6 см в диаметре. Локализация АВМ в функционально значимом участке головного мозга (например, речевые, двигательные, чувствительные или зрительные центры) добавляет 1 балл. Также присваивается 1 дополнительный балл, если АВМ дренируется в глубокие вены мозга. Обычно АВМ, набирающие 4 и более баллов по этой шкале, считаются недоступными для прямого хирургического лечения. В 42-47 % случаев разрыв АВМ осложняется развитием внутричерепных гематом на фоне субарахноидальных и(или) внутрижелудочковых кровоизлияний [25]. Для оценки тяжести геморрагического инсульта, несмотря на преимущественное использование в оценке тяжести разрыва церебральных аневризм, используется шкала W. Hunt, R. Hess (1968) (таблица 1).
Таблица 1 - Шкала тяжести состояния больных в остром периоде субарахноидального кровоизлияния (по W. Hunt, R. Hess, 1968)
I степень тяжести Бессимптомное течение, возможна слабовыраженная головная боль или ригидность мышц затылка
II степень тяжести головная боль умеренная или слабовыраженная, менингеальный синдром выражен, очаговая неврологическая симптоматика отсутствует, за исключением возможного поражения глазодвигательных нервов
III степень тяжести менингеальный синдром выражен, сознание расстроено до оглушения, очаговая симптоматика умеренно выражена
IV степень тяжести менингеальный синдром выражен, сознание расстроено до сопора, очаговая симптоматика выражена, имеются признаки нарушения витальных функций
V степень тяжести кома различной глубины, акинетический мутизм, децеребрационная ригидность
Как уже говорилось выше, к основным факторам риска кровотечения из мальформации относятся: ранее перенесенное кровоизлияние, единственная дренирующая вена, диффузное строение АВМ, участие оболочечных артерий в их кровоснабжении. Частота повторных кровотечений при АВМ глубинной локализации с распространением на подкорковые узлы составляет 40,9 %, в то время как при поверхностных АВМ - 32,5 %. При дренировании мальформации в глубокие вены повторные кровоизлияния развиваются у 34,2 % больных, а при поверхностном дренировании - у 2,6 %. Статистически достоверной является зависимость риска кровоизлияния от величины АВМ: при размере менее 3 см в диаметре кровоизлияния развиваются у 86,7 % пациентов, от 3 до 6 см - у 72,7 %, свыше 6 см — в 30,8 % [21, 69].
Одно из крупнейших исследований по артериовенозным мальформациям ARUBA показывает ежегодный риск кровотечения вследствие разрыва АВМ 2,2 % [28]. Риск возникновения кровоизлияния сохраняется в течение всей жизни. Летальность от первого кровоизлияния варьирует от 10 до 30 %, инвалидизация достигает 50 % [41, 95]. Риск повторного кровоизлияния, особенно в течение первого года, несколько выше и по данным разных исследований варьирует от 6 % до 32,9 % [56, 61, 67], со снижением в последующие годы до исходного уровня. Индивидуальный риск кровоизлияния у пациента-носителя АВМ в течение жизни может быть ориентировочно определен по формуле [105, 112]:
где X - риск кровоизлияния в течение оставшихся лет жизни, а - ежегодный риск кровоизлияния (0,03), b - прогнозируемый оставшийся срок жизни (в годах).
Помимо самого факта наличия АВМ выявлены анатомо-физиологические факторы - предикторы более высокого риска кровоизлияния. К их числу традиционно относят [54, 100]:
1) высокое давление крови в клубке мальформации за счет особенностей строения питающих артерий или нарушения венозного оттока от АВМ,
2) наличие аневризм в составе клубка АВМ (интранидальные аневризмы),
3) глубинная паравентрикулярная или внутрижелудочковая локализация
4) малый размер АВМ.
Торпидный тип. Торпидный или пседотуморозный тип течения у пациентов с АВМ головного мозга встречается по данным разных авторов от 20 % до 67 % [46, 108, 109]. Данный тип течения характеризуется развитием судорожного синдрома, кластерных головных болей, симптоматики прогрессирующего неврологического дефицита. Чаще всего наблюдаются симптоматические судорожные припадки (до 67 % всех АВМ головного мозга).
Судорожные приступы могут быть как следствием кровоизлияния из-за разорвавшейся мальформации, так и присутствовать у человека с неразорвавшейся АВМ в течение многих лет [105]. Всемирной организацией здравоохранения (ВОЗ) определено понятие эпилепсия как хроническое неврологическое заболевание, характеризующееся рецидивирующими припадками, то есть непроизвольными движениями части или всего тела, которые могут или не могут сопровождаться потерей сознания и потерей контроля над функцией кишечника и мочевого пузыря (Всемирная организация здравоохранения, 2016 г.). Также, по данным ВОЗ, эпилепсией считается наличие в анамнезе 2 и более эпилептических приступа, и только в этом случае пациенту назначаются противоэпилептические препараты (ПЭП). В отношении с больными с церебральными АВМ наличие патологического очага в головном мозге позволяет предполагать развитие повторных эпилептических приступов после развития первого и, в данном случае, назначение ПЭП оправдано после одного судорожного приступа. Кроме того, структурная эпилепсия при церебральных АВМ имеет преимущественно фармакорезистентное течение (до 75 %) [14, 20]. По определению противоэпилептической лиги фармакорезистентная эпилепсия
определяется как неудача использования правильно подобранных не менее двух противосудорожных препаратов, будь то в монотерапии или их комбинации для достижения свободы от приступов [50]. Эпилептический тип течения до сих пор считается менее опасным в отношении развития кровоизлияния вследствие разрыва АВМ. Однако, эпилептические приступы значительно снижают качество жизни данной группы больных, в том числе ограничивают их социальную и профессиональную активность, увеличивают риски несчастных случаев и травматизма, ограничивают занятия спортом (плавание, альпинизм и т. д.), кроме того данный тип течения обязывает больных к постоянному приему противосудорожной терапии и принимать все побочные эффекты этих препаратов.
Считается, что торпидный тип течения более характерен для АВМ высокой градации по Spetzler - Martin [85]. Кроме того, сосудистый клубок обладает раздражающим действием на головной мозг и может вызывать эффект обкрадывания структур мозга, вызывая прогрессирование неврологического дефицита [6, 7, 14, 20, 24, 27].
Рядом разных авторов [56, 60, 61] определены параметры АВМ, с наибольшей вероятностью которые могут вызвать развитие эпилептических приступов, такие как:
1) расположение АВМ в коре головного мозга,
2) крупные АВМ (> 3 см),
3) АВМ, питающиеся из СМА (средней мозговой артерии),
4) отсутствие интранидальных аневризм,
5) наличие варикозов в венозном дренаже.
По данным литературы, на сегодняшний день многие авторы утверждают, что наилучшую свободу от эпилептических приступов позволяет достичь микрохирургическое удаление мальформации головного мозга. Однако число избавленных от припадков после хирургического лечения широко варьирует от 4 до 83 % [67, 108, 111, 116, 119, 120]. Развитие хирургических технологий
позволяет надежно получать высокие проценты исцеления после микрохирургической резекции - 78 % в серии АВМ I-III градации по SM [38], 77 % в серии АВМ I-V градации по SM [75]. В то же самое время хирургия АВМ головного мозга сопряжена с риском появления припадков de-novo у больных, у которых их не было до операции. Процент такого исхода варьирует от 3 до 31,6 % [68, 91, 111, 116]. И даже 35,7 % в серии из 164 пациентов в работе J. Y. Wang и соавт. [71]. Хирургическое лечение может провоцировать появление новых эпилептогенных очагов, вследствие манипуляций на паренхиме мозга и его сосудах во время резекции АВМ [43]. У больных с АВМ высоких градаций по SM хирургическая резекция сопряжена с высокой послеоперационной инвалидизацией и летальностью [117].